Сон разума рождает чудовищ
Ф.Гойя
Сон разума рождает чудовищ
Ф.Гойя
|
|
Синтез пуриновых нуклеотидов осуществляется из инозинмонофосфата (ИМФ). Азотистое основание ИМФ гипоксантин превращается в аденин (первая стадия) и в гуанин (вторая стадия). Так образуются нуклеозидмонофосфаты АМФ и ГМФ, которые превращаются в нуклеозиддифосфаты АДФ и ГДФ.
Процесс контролируется нуклеозидфосфаткиназами. Под действием нуклеозиддифосфаткиназ АДФ и ГДФ превращаются в АТФ и ГТФ. Нуклеозидтрифосфаты используются либо для построения РНК, либо в качестве коферментов. Преобразование рибонуклеотидов в дезоксирибонуклеотиды происходит на стации дифосфатов и катализируется нуклеозиддифосфатредуктазой.
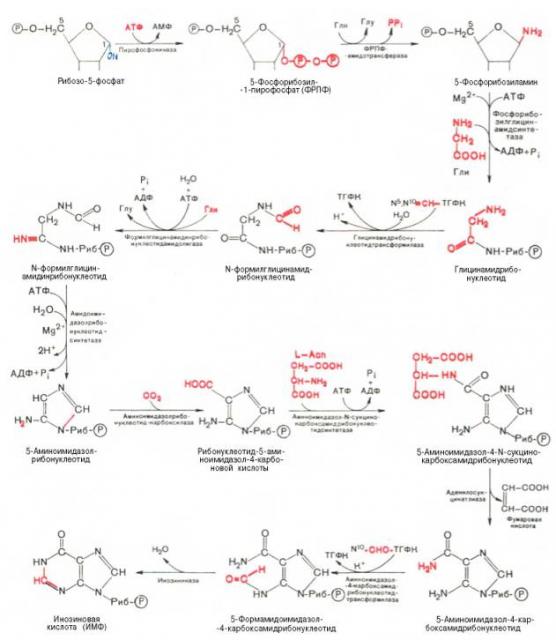
Атомы углерода 4 и 5, атом азота 7 имеют своим источником глицин, атомы азота 3 и 9 – амидную группу глутамина, атом азота 1 – аспарагиновую кислоту. Атом углерода 2 происходит из формил-ТГФК (5,6,7,8-тетрагидрофолиевой кислоты), атом углерода 8 – из метенил-ТГФК, атом углерода 6 – из углекислого газа. Пути биосинтеза пуриновых нуклеотидов в печени животных и у многих микроорганизмов (Е. coli и Neurospora crassa), почти полностью совпадает.
Конечный результат синтеза – не свободное пуриновое основание, а рибонуклеотид инозиновая кислота (ИМФ).
Синтез ИМФ начинается с D-рибозо-5-фосфата, являющегося продуктом пентозофосфатного цикла. На D-рибозо-5-фосфат переносится фосфогруппа с АТФ. Образуется 5-фосфорибозил-1-пирофосфат, который взаимодействует с глутамином с образованием β-5-фосфорибозиламина. Это ключевая стадия в синтезе пуринов. На следующей стадии к свободной NH2-группе β-5-фосфорибозиламина присоединяется молекула глицина, и образуется глицинамидрибонуклеотид. На следующей стадии присоединяется формильная группа N5,N10-метенил-ТГФК, и образуется формилглицинамидрибонуклеотид.
На формильную группу формилглицинамидрибонуклеотида переносится амидная группа глутамина, и образуется формилглицинамидинрибонуклеотид. Затем пятичленное имидазольное кольцо замыкается с образованием 5-аминоимидазолрибонуклеотида, способного акцептировать СО2 с образованием 5-аминоимидазол-4-карбоновой кислоты.
В последующем двухступенчатом процессе, в котором участвуют аспа-рагиновая кислота и АТФ, образуется 5-аминоимидазол-4-карбоксамид-рибонуклеотид с освобождением фумаровой кислоты. Азот аспарагиновой кислоты становится в 1-е положение будущего пуринового ядра. Последний углеродный атом пиримидинового кольца пурина вводится в виде формильного остатка, присоединяющегося к 5-NH2-группе. Наконец, отщепляется молекула воды, и образуется ИМФ.
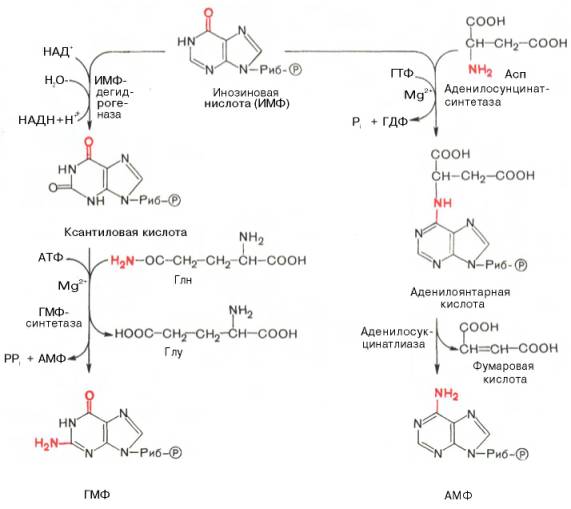
АМФ и ГМФ образуются из ИМФ, причем в синтезе обоих мононуклеотидов участвуют по два фермента. Образование ГМФ катализируют ИМФ-дегидрогеназа и ГМФ-синтетаза, образование АМФ – аденилосукцинатсинтетаза и аденилосукцинатлиаза.
В ферментативном синтезе АМФ из ИМФ в качестве донора NH2-группы участвует аспарагиновая кислота. Источником энергии служит ГТФ. Промежуточный продукт – янтарная кислота.
Биосинтез ГМФ начинается с превращения ИМФ в ксантозиловую кислоту (реакция контролируется ИМФ-дегидрогеназой), которая аминируется с участием амидного азота глутамина.
Превращение АМФ и ГМФ в соответствующие нуклеозидди- и нуклео-зидтрифосфаты также протекает в 2 стадии при участии специфических нуклеозидмонофосфат- и нуклеозиддифосфаткиназ :
ГМФ + АТФ <=> ГДФ + АДФ
ГДФ + АТФ <=> ГТФ + АДФ
Синтез пуриновых нуклеотидов тормозится конечными продуктами по принципу обратной связи, т.е. ингибированием переноса аминогруппы глутамина на 5-фосфорибозил-1-пирофосфат.
Кроме того, избыток ГМФ в клетках оказывает аллостерическое торможение только на свой собственный синтез, не влияя на синтез АМФ; накопление АМФ подавляет свой синтез, не ингибируя синтез ГМФ.
Наш твиттер
ВУЗы |
Ресурс содержит материалы 12+